دليل طبي شامل عن التليف الكيسي: أسبابه الجينية، أعراضه في الرئة والجهاز الهضمي، طرق التشخيص بفحص العرق والجينات، وأحدث علاجات معدلات CFTR التي رفعت متوسط العمر المتوقع إلى 50 عاماً.
⚡ الإجابة السريعة
ما هو التليف الكيسي؟
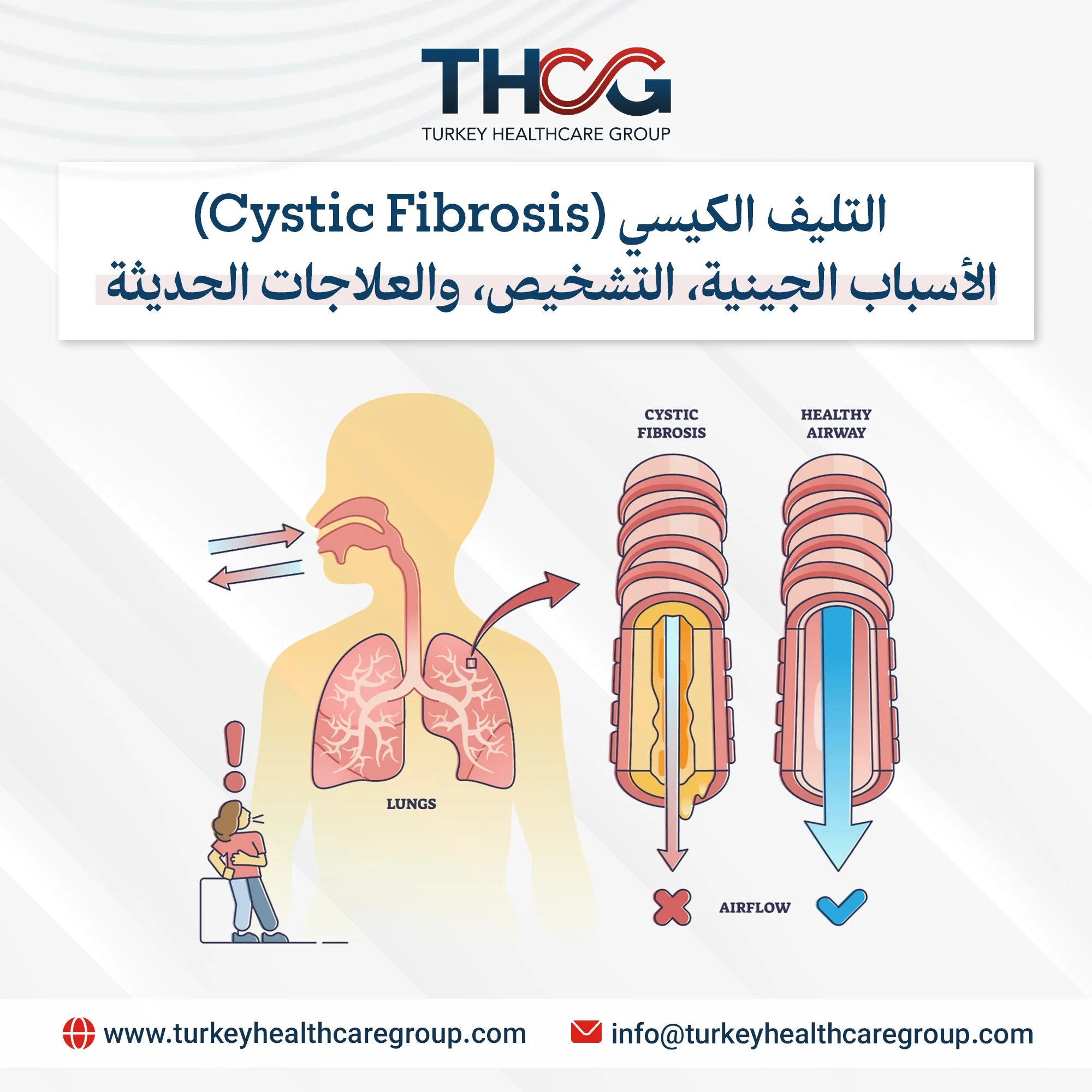
التليف الكيسي (Cystic Fibrosis) هو اضطراب جيني وراثي متنحٍ ناتج عن خلل في جين
CFTR المسؤول عن تنظيم توازن الأملاح والسوائل في خلايا الجسم. يؤدي هذا الخلل إلى
تراكم مخاط سميك ولزج في الرئتين والجهاز الهضمي والأعضاء الأخرى، مما يسبب التهابات متكررة
وتدهوراً تدريجياً في وظائف الرئة وقصور البنكرياس.
| السبب | طفرة في جين CFTR — الأكثر شيوعاً F508del |
| الأعراض الرئيسية | سعال مزمن، التهابات رئوية متكررة، قصور البنكرياس، سوء الامتصاص |
| التشخيص | فحص الكلوريد في العرق + الاختبار الجيني + مسح حديثي الولادة |
| العلاج الحديث | معدلات CFTR (Trikafta) — تحسّن الوظائف وتقلل التفاقمات بأكثر من 60% |
| متوسط العمر المتوقع | يتجاوز 50 عاماً في البيئات ذات الرعاية المتقدمة |
جدول المحتويات
Toggleالتليف الكيسي (Cystic Fibrosis) الأسباب الجينية، التشخيص، والعلاجات الحديثة
ما هو التليف الكيسي؟
يُعد التليف الكيسي اضطراباً جينياً وراثياً متنحياً، وهو مرض تدريجي متعدد الأجهزة شهد تحولاً جذرياً خلال العقد الماضي؛ حيث تغير من كونه مرضاً قاتلاً في مرحلة الطفولة إلى حالة مزمنة يمكن التعايش معها. فبعد أن كان التليف الكيسي يُعرف قديماً بالفشل التنفسي المبكر وسوء التغذية الحاد، يتجاوز متوسط العمر المتوقع للمصابين به اليوم 50 عاماً في البيئات ذات الموارد العالية،
وهو تقدم مدفوع بشكل كبير بتطور فحص حديثي الولادة، والرعاية المكثفة متعددة التخصصات، والاعتماد الواسع لعلاجات مُعدِّلات بروتين منظم التوصيل عبر الغشاء في التليف الكيسي (CFTR). يقدم هذا المقال نظرة شاملة وقائمة على الأدلة حول التليف الكيسي، مصممة للأطباء، والممارسين الصحيين المساعدين، والمرضى المطلعين الذين يواكبون الرعاية الحديثة لهذا المرض.
الوراثة والفيزيولوجيا المرضية الجزيئية
يحدث التليف الكيسي بسبب متغيرات ممرضة في جين (CFTR)، الواقع على الذراع الطويلة للكروموسوم 7 (7q31.2). يشفر هذا الجين بروتيناً يتكون من 1,480 حمضاً أمينياً، يعمل كقناة للكلوريد والبيكربونات ينظمها أحادي فوسفات الأدينوسين الحلقي (cAMP)، ويتم التعبير عنها بشكل أساسي في الأغشية القمية للخلايا الظهارية المبطنة للجهاز التنفسي، والبنكرياس، والجهاز الكبدي المراري، والأمعاء، والغدد العرقية، والقنوات التناسلية. ومنذ اكتشافه في عام 1989، تم تصنيف أكثر من 2,100 متغير في جين (CFTR)، منها أكثر من 400 متغير مسبب للمرض.
ويعتبر المتغير (F508del) الأكثر انتشاراً، حيث يمثل حوالي 70% من أليلات التليف الكيسي في جميع أنحاء العالم. يتسبب هذا المتغير في سوء طي بروتين (CFTR)، مما يؤدي إلى تحلله المبكر بواسطة “البروتيزوم” قبل وصوله إلى سطح الخلية. وتنتج المتغيرات الأخرى بروتينات (CFTR) تعاني من ضعف في فتح القنوات، أو انخفاض في التصنيع، أو تغير في التوصيل، أو سرعة في التلف. تاريخياً، صُنفت طفرات (CFTR) إلى ست فئات وظيفية (I–VI)، تتراوح من الغياب التام لإنتاج البروتين (الفئة I) إلى انخفاض استقرار البروتين على الغشاء (الفئة VI). ورغم أن نظام التصنيف هذا ليس مثالياً، إلا أنه يظل مفيداً سريرياً للتنبؤ بالاستجابة العلاجية، لا سيما لمُعدِّلات (CFTR).
يتمثل الخلل الفيزيولوجي المرضي الأساسي في التليف الكيسي في ضعف إفراز الكلوريد والبيكربونات مقترناً بزيادة امتصاص الصوديوم عبر قناة الصوديوم الظهارية (ENaC). ويؤدي عدم التوازن في نقل الأيونات إلى تجفيف السائل المبطن لسطح المسالك الهوائية، مما يعيق التصفية المخاطية الهدبية. فتتراكم إفرازات سميكة ولزجة تخلق بيئة غنية بالمغذيات ولا هوائية، مما يعزز الاستعمار البكتيري المزمن، والالتهاب العدلي المستمر (neutrophilic inflammation)، وتدمير الأنسجة التدريجي. ومع مرور الوقت، تؤدي العدوى والالتهابات المتكررة إلى توسع القصبات، وإعادة تشكيل الممرات الهوائية، وتدهور لا رجعة فيه في وظائف الرئة. وخارج الرئتين، يؤدي انسداد الغدد الخارجية إلى قصور البنكرياس، وأمراض الكبد والمرارة، واضطرابات حركة الأمعاء، وعقم الذكور الناجم عن الغياب الخلقي الثنائي للأسهر (CBAVD).
ما هي أعراض مرض التليف الكيسي؟
يظهر التليف الكيسي تبايناً ظاهرياً كبيراً، يتأثر بالنمط الجيني لـ (CFTR)، والتعرضات البيئية، والجينات المعدلة، والقدرة على الوصول إلى الرعاية المتخصصة. وعادة ما تهيمن المظاهر التنفسية على المسار السريري؛ حيث يعاني المرضى غالباً من سعال منتج مزمن، وأزيز، وعدم تحمل الجهد البدني، وعدون تنفسية رئوية متكررة. وتشمل الممرضات المبكرة غالباً “المكورات العنقودية الذهبية” و”المستدمية النزلية”، لكن استعمار “الزائفة الزنجارية” المزمن يظهر في سن المراهقة أو بداية البلوغ ويرتبط ارتباطاً وثيقاً بالتدهور المتسارع لوظائف الرئة.
وتشمل الممرضات الأخرى البارزة أنواع “الستينوتروفوموناس” و”الأكروموباكتر”، ومجموعة “بورخولدرية بصلية”، والمتفطرات غير السلية (NTM). كما تعد التهابات الجيوب الأنفية المزمنة، والزوائد الأنفية، وداء الرشاشيات القصبي الرئوي الأرجي (ABPA) من الأمراض المصاحبة الشائعة.
وتعتبر المظاهر الهضمية والغذائية على نفس القدر من الأهمية؛ حيث يصاب حوالي 85-90% من الأفراد المصابين بالتليف الكيسي بقصور البنكرياس الخارجي (PEI)، والذي يتميز بسوء امتصاص الدهون، والإسهال الدهني، وانتفاخ البطن، ونقص الفيتامينات القابلة للذوبان في الدهون (A, D, E, K). ويؤدي قصور البنكرياس غير المعالج إلى فشل النمو، وهشاشة العظام، واعتلال التخثر. قد يظهر لدى حديثي الولادة “علوص ميكونيوم” (انسداد الأمعاء بالعقي)، وهو عرض مرضي مميز ناتج عن إفرازات معوية متصلبة. أما المرضى الأكبر سناً فهم عرضة لخطر متلازمة الانسداد المعوي البعيد (DIOS)، ومرض الارتجاع المعدي المريئي، وأمراض الكبد المرتبطة بالتليف الكيسي، والتي تتراوح من ارتفاع إنزيمات الكبد الصامت إلى التليف المراري البؤري وارتفاع ضغط الدم البابي.
وعادة ما يظهر مرض السكري المرتبط بالتليف الكيسي (CFRD) في العقد الثاني أو الثالث من العمر، ويمثل مزيجاً فريداً من نقص الأنسولين (بسبب تليف البنكرياس وفقدان خلايا الجزيرة) ومقاومة الأنسولين (التي تتفاقم بسبب الالتهاب المزمن واستخدام الكورتيكوستيرويدات). ويرتبط هذا النوع من السكري بتدهور الحالة التغذوية، وتسارع تدهور الرئة، وزيادة الوفيات، مما يستلزم إجراء فحص روتيني سنوياً عن طريق اختبار تحمل الجلوكوز الفموي بدءاً من سن العاشرة.
كما تتأثر الصحة الإنجابية بشكل كبير؛ فتقريباً جميع الذكور المصابين بالتليف الكيسي يعانون من العقم بسبب (CBAVD)، رغم أن إنتاج الحيوانات المنوية يكون طبيعياً في الغالب، مما يسمح بالتكاثر الناجح عبر استخراج الحيوانات المنوية من الخصية والحقن المجهري. أما لدى الإناث، فتقل الخصوبة بسبب سماكة مخاط عنق الرحم وتغير وظائف الأنابيب، ومع ذلك، أصبح الحمل شائعاً بشكل متزايد ويمكن تحمله بشكل جيد عموماً لدى النساء اللواتي يتمتعن بوظائف رئة مستقرة (FEV1 > 50% من المتوقع) وتغذية محسنة.
كيف يتم تشخيص مرض التليف الكيسي؟
يُعد التشخيص المبكر أمراً حيوياً للحفاظ على وظائف الرئة والحالة التغذوية. أصبح المسح الشامل لحديثي الولادة (NBS) للكشف عن التليف الكيسي معياراً قياسياً الآن في الولايات المتحدة وكندا وأوروبا وأستراليا والعديد من المناطق الأخرى. تعتمد الخوارزمية الأكثر انتشاراً قياس “مولد التريبسين المناعي” (IRT) من بقع الدم المجففة، يليه تحليل مستهدف للحمض النووي لجين (CFTR) أو اختبار (IRT) ثانٍ إذا كانت القيمة الأولية مرتفعة. وتتطلب نتائج المسح الإيجابية إحالة سريعة إلى مركز معتمد للتليف الكيسي لإجراء الاختبارات التأكيدية.
يظل اختبار الكلوريد في العرق بطريقة الرحلان الأيوني للبلوربين الكمي هو المعيار الذهبي للتشخيص. وتكون النتائج كالتالي:
- تركيز كلوريد العرق ≥ 60 مليمول/لتر: مؤشر لتشخيص التليف الكيسي.
- القيم بين 30-59 مليمول/لتر: قيم غير محددة وتستدعي الربط الجيني والسريري.
- القيم < 30 مليمول/لتر: تستبعد التليف الكيسي بشكل عام.
تحدد الاختبارات الجينية المتغيرات المسببة للمرض في جين (CFTR) وتوجه أهلية المريض للعلاجات المُعدِّلة. ويُوصى باستخدام لوحات جينية شاملة أو تسلسل الجيل التالي (NGS) عندما تكون نتائج اختبار العرق غامضة أو عندما يظل الشك السريري مرتفعاً رغم النتائج الحدودية.
وتشمل التقييمات الأساسية الإضافية قياس التنفس (أو اختبار وظائف الرئة للرضع عند الإمكان)، وتصوير الصدر (الأشعة المقطعية عالية الدقة أو الرنين المغناطيسي لتقييم توسع القصبات المبكر)، وزراعة البلغم أو مسحات البلعوم، واختبار “إيلاستاز-1” في البراز (لقياس وظائف البنكرياس)، ومستويات الفيتامينات القابلة للذوبان في الدهون، والمقاييس البشرية الغذائية. ومع تقدم المرضى في السن، يصبح الفحص الروتيني لسكري التليف الكيسي (CFRD)، وكثافة المعادن في العظام، ووظائف الكبد، والاضطرابات النفسية جزءاً لا يتجزأ من الرعاية الشاملة.
كيف يتم علاج مرض التليف الكيسي؟
تعتمد الإدارة الحديثة للتليف الكيسي على مراكز رعاية معتمدة متعددة التخصصات تجمع بين أمراض الرئة، والجهاز الهضمي، والغدد الصماء، والتغذية، والعلاج التنفسي، والصيدلة، وعلم النفس، والخدمة الاجتماعية. العلاج فردي للغاية، يعتمد على النمط الجيني، ويركز على الحفاظ على وظائف الأعضاء، ومنع المضاعفات، وتحسين جودة الحياة.
تصفية المسالك الهوائية والعلاج التنفسي
تظل تقنيات تصفية المسالك الهوائية اليومية (ACTs) أساسية، وتشمل الخيارات:
- العلاج الطبيعي للصدر مع نزح الوضعية والقرع.
- أجهزة ضغط الزفير الإيجابي (PEP).
- أجهزة (PEP) المتذبذبة (مثل Flutter و Acapella).
- سترات تذبذب جدار الصدر عالية التردد.
- النزح الذاتي. ويُنصح بشدة بممارسة الرياضة كعامل مساعد طبيعي لهذه التقنيات، حيث تعمل على تحسين التهوية وتصفية البلغم واللياقة القلبية الوعائية.
تعزز الأدوية الحالة للمخاط من طرد البلغم؛ حيث يعمل “دورناز ألفا” المستنشق (DNase البشري المؤتلف) على تكسير الحمض النووي خارج الخلايا، مما يقلل من لزوجة البلغم. كما يعمل المحلول الملحي عالي التركيز (3-7%) على سحب المياه أسموزياً إلى تجويف المسالك الهوائية. وعادة ما تُعطى هذه العوامل بعد موسعات الشعب الهوائية لتخفيف التشنج القصبي.
التحكم بالعدوى والإشراف على مضادات الميكروبات
تتطلب عدوى المسالك الهوائية المزمنة إدارة استباقية موجهة بالزراعة المخبرية. وتستدعي التفاقمات الرئوية الحادة (التي تُعرف بزيادة السعال، أو حجم البلغم، أو ضيق التنفس، أو التعب، أو انخفاض FEV1) علاجاً سريعاً بالمضادات الحيوية. ولتثبيط بكتيريا “الزائفة الزنجارية” المزمنة، يُستخدم عادة التناوب بين التوبراميسين المستنشق، أو أزتريونام لايسين، أو كوليستيميثات. وتُستخدم “الماكروليدات” (مثل أزيثروميسين 3 مرات أسبوعياً) لخصائصها المعدلة للمناعة والمضادة للغشاء الحيوي (Biofilm).
حدثت ثورة في رعاية التليف الكيسي مع إدخال مُعدِّلات (CFTR)، وهي أدوية تستهدف خلل البروتين الأساسي.
- إيفاكافتور (Ivacaftor): “مُقوٍّ” يحسن فتح القنوات.
- المصححات (Lumacaftor, Tezacaftor, Elexacaftor): تسهل الطي الصحيح وانتقال بروتين (F508del-CFTR) إلى سطح الخلية.
العلاج الثلاثي (Elexacaftor/Tezacaftor/Ivacaftor) المعروف تجارياً باسم (Trikafta/Kaftrio) معتمد للأفراد من عمر 6 أشهر فما فوق الذين لديهم أليل (F508del) واحد على الأقل، مما يشمل حوالي 90% من مرضى التليف الكيسي. وأظهرت التجارب تحسناً مستداماً في (FEV1) بنسبة 10-15 نقطة مئوية، وتقليل التفاقمات الرئوية بنسبة تزيد عن 60%.
الوقاية من خلال التغذية والجهاز الهضمي
ترتبط التغذية المثالية ارتباطاً وثيقاً بالنتائج الرئوية. يحتاج المرضى إلى وجبات عالية السعرات والدهون (110-200% من المخصصات اليومية الموصى بها) مدعومة بعلاج تعويض إنزيمات البنكرياس (PERT) الذي يُؤخذ مع جميع الوجبات. كما يتم علاج سكري التليف الكيسي (CFRD) باستخدام أنظمة الأنسولين (Basal-bolus) والمراقبة المستمرة للجلوكوز، حيث إن خافضات السكر الفموية غير فعالة عموماً.
تطور مرض التليف الكيسي وزراعة الرئة
رغم العلاج الأمثل، تتقدم حالة بعض المرضى إلى المرحلة النهائية من مرض الرئة. تشمل دواعي زراعة الرئة انخفاض (FEV1) لأقل من 30%، أو التدهور السريع، أو نفث الدم المتكرر. وتتجاوز نسبة البقاء على قيد الحياة بعد الزرع 70% عند 5 سنوات، مع استمرار الحاجة للمتابعة متعددة التخصصات لعلاج مضاعفات التليف الكيسي غير الرئوية.
أصبح فحص الصحة العقلية الآن معياراً للرعاية، حيث يؤثر الاكتئاب والقلق وعبء العلاج على 30-40% من المراهقين والبالغين المصابين، وتساهم الخدمات النفسية المتكاملة وأدوات الصحة الرقمية في تحسين الالتزام بالعلاج والتكيف مع المرض.
المضاعفات والأمراض المصاحبة
بعيداً عن توسع القصبات التدريجي والفشل التنفسي، يواجه مرضى التليف الكيسي مضاعفات في أجهزة متعددة:
- اعتلال المفاصل المرتبط بالتليف الكيسي: يظهر كألم مفصلي نوبي أو مزمن، وغالباً ما يكون سلبياً للمصل (seronegative) ويستجيب لمضادات الالتهاب غير الستيرويدية (NSAIDs).
- صحة العظام: تؤدي هشاشة العظام ونقص فيتامين D إلى الاستعداد لكسور الهشاشة، ويتم التخفيف من ذلك عبر تمارين تحمل الوزن، ومكملات الكالسيوم وفيتامين D، والبيسفوسفونات عند الحاجة.
- أمراض الكبد والقنوات المرارية: تتقدم بشكل خفي؛ وقد يحسن حمض “أورسوديوكسيكوليك” إنزيمات الكبد لكنه لا يوقف التليف. وقد تتطلب حالات أمراض الكبد المتقدمة زراعة الكبد.
تتطلب مخاطر العدوى المتبادلة، ومقاومة المضادات الحيوية، ومضاعفات تعدد الأدوية إشرافاً دقيقاً. كما يفرض تقدم عمر مجتمع التليف الكيسي تحديات جديدة، مثل أمراض القلب والأوعية الدموية، وفحوصات السرطان، والتفاعلات الدوائية للمعدِّلات، مما يستلزم تحديث الإرشادات السريرية وخبرات طب كبار السن الخاصة بالتليف الكيسي.
أبحاث متقدمة وتوجهات مستقبلية (رؤية 2026)
انتقل البحث في التليف الكيسي من إدارة الأعراض إلى تعديل المرض والشفاء الوظيفي:
- تقنيات تحرير الجينات: بما في ذلك CRISPR-Cas9 ومحررات القواعد، والتي تخضع حالياً لتجارب سريرية تهدف لتصحيح طفرات (CFTR) على المستوى الجينومي.
- أنظمة توصيل mRNA: يتم تحسينها لاستهداف الخلايا الظهارية للمسالك الهوائية، مما يوفر أملاً للمرضى الذين يعانون من طفرات لا تستجيب للمعدِّلات الحالية.
- علاجات الميكروبيوم: بما في ذلك البروبيوتيك المهندس، وزراعة الميكروبيوم المعوي، والجسيمات النانوية المضادة للغشاء الحيوي لكسر دورات العدوى المزمنة.
- الذكاء الاصطناعي: يتم دمجه للتنبؤ بالتفاقمات، وتحسين تقنيات تصفية المسالك الهوائية بشكل شخصي، والمراقبة عن بعد عبر قياس التنفس القابل للارتداء.
تستمر نتائج الحمل في التحسن، حيث تؤكد السجلات سلامة المعدِّلات مع التوصية باستمرارها طوال فترة الحمل. كما تعمل المبادرات الصحية العالمية على توسيع برامج مسح حديثي الولادة والتفاوض على أسعار متدرجة للمعدِّلات لتقليص فجوة البقاء على قيد الحياة عالمياً.
لقد تحسن إنذار التليف الكيسي بشكل كبير؛ ففي البلدان التي يتوفر فيها المسح الشامل لحديثي الولادة، والرعاية المتخصصة، والوصول للمعدِّلات، يتجاوز متوسط البقاء الآن 50 عاماً، ويعيش العديد من المرضى حتى العقدين السادس والسابع. كما تباطأ انخفاض (FEV1)، وانخفض تكرار التفاقمات، واستقرت المعايير الغذائية لدى معظم المرضى الملتزمين بالعلاج. وتحسنت مقاييس جودة الحياة بشكل ملحوظ، بما في ذلك الحضور الدراسي، والتوظيف، وتكوين الأسرة.
ومع ذلك، يظل التليف الكيسي مرضاً مزمناً مرهقاً؛ إذ تتطلب أنظمة العلاج اليومية عادة من 2 إلى 4 ساعات، مما يؤثر على التعليم والوظيفة والحياة الاجتماعية. كما تعد فترة الانتقال من رعاية الأطفال إلى رعاية البالغين مرحلة حرجة تتطلب برامج مهيكلة لمنع حدوث فجوات في الرعاية. وتستمر التفاوتات الصحية؛ إذ تواجه المجتمعات المهمشة والمناطق منخفضة الدخل تأخراً في التشخيص ومحدودية في الوصول للعلاج، مما يجعل معالجة هذه المظالم أولوية قصوى لجهود المناصرة والسياسات الصحية في عام 2026 وما بعده.
يجسد التليف الكيسي انتصار الطب الانتقالي؛ فمن اكتشاف الجين إلى التصحيح البروتيني المستهدف، تطورت رعاية المرضى لتصبح نموذجاً للإدارة الدقيقة والمتمركزة حول المريض. وبينما غيّرَت مُعدِّلات (CFTR) مسار المرض بشكل كبير، تظل الرعاية الشاملة ضرورية. إن الأبحاث المستمرة في العلاج الجيني وتعديل الميكروبيوم والوصول العادل للعلاج تعد بتحول أكبر، مع الهدف النهائي المتمثل في الشفاء الوظيفي لجميع الأنماط الجينية. في العصر الحديث، يتطلب التليف الكيسي الاحتفاء بالتقدم غير المسبوق مع التزام راسخ بالعمل اليومي للعيش بشكل جيد مع هذه الحالة الوراثية المعقدة.
الأسئلة الأكثر بحثاً
كل ما تريد معرفته عن التليف الكيسي
إجابات دقيقة وموثوقة على أكثر الأسئلة شيوعاً حول التليف الكيسي —
من التشخيص والأعراض إلى أحدث العلاجات وفرص الحياة الطبيعية.
س1: هل التليف الكيسي مرض نادر؟
ج: هو ليس نادراً بمعنى الأمراض النادرة جداً، لكنه غير شائع. يُعدّ أكثر الاضطرابات الجينية الوراثية المهددة للحياة انتشاراً بين ذوي الأصول الأوروبية. على مستوى العالم يُصاب به نحو 100,000 شخص، ويظل أقل تشخيصاً في مناطق كثيرة بسبب محدودية برامج الفحص الوراثي.
س2: كيف يرث الطفل مرض التليف الكيسي؟
ج: التليف الكيسي وراثي متنحٍ، أي يحتاج الطفل لوراثة نسختين معيبتين من جين CFTR — واحدة من كل والد. إذا كان الوالدان حاملين للجين المعيب (غير مصابين)، فاحتمال إصابة كل طفل 25%، واحتمال كونه حاملاً 50%، واحتمال سلامته الكاملة 25%.
س3: ما هي أولى علامات التليف الكيسي عند الرضيع؟
ج: أبرز العلامات المبكرة: انسداد الأمعاء بالعقي (علوص ميكونيوم) فور الولادة، ملوحة غير عادية في جلد الطفل عند التقبيل، سعال مزمن وصفير تنفسي، وفشل في النمو رغم الرضاعة الجيدة. فحص مسح حديثي الولادة يكشف المرض قبل ظهور الأعراض في البلدان التي تعتمده.
س4: ما هو فحص الكلوريد في العرق ولماذا هو المعيار الذهبي للتشخيص؟
ج: هو اختبار يقيس تركيز الكلوريد في عرق المريض بعد تحفيز الغدد العرقية كيميائياً. يُعدّ معياراً ذهبياً لأن خلل CFTR يؤثر مباشرةً على الغدد العرقية، فيرتفع الكلوريد بشكل مميز. نتيجة ≥60 مليمول/لتر تؤكد التشخيص، وأقل من 30 تستبعده في الغالب.
س5: هل الاختبار الجيني يغني عن فحص العرق؟
ج: لا، كلاهما مكمّل للآخر. الاختبار الجيني يحدد الطفرة المحددة في جين CFTR ويوجه خيارات العلاج. أما فحص العرق فيؤكد أن الطفرة تؤثر فعلياً على وظيفة البروتين. في حالات غير واضحة يُستخدم تسلسل الجيل التالي (NGS) للتحليل الشامل.
س6: ما الفرق بين مريض التليف الكيسي وحامل الجين؟
ج: حامل الجين لديه نسخة واحدة معيبة ونسخة سليمة، فيعمل الجين السليم بكفاءة تامة ولا تظهر عليه أعراض المرض مطلقاً. لكنه قادر على نقل الجين المعيب لأطفاله. المصاب يملك نسختين معيبتين فتختل وظيفة CFTR وتظهر الأعراض.
س7: لماذا تُعدّ الرئة الأكثر تضرراً في التليف الكيسي؟
ج: لأن خلل CFTR يعيق التصفية المخاطية الهدبية في المسالك الهوائية، فيتراكم مخاط سميك يخلق بيئة مثالية لنمو البكتيريا مثل الزائفة الزنجارية. الالتهابات المتكررة تُشعل استجابة مناعية مستمرة تتلف الأنسجة تدريجياً وتؤدي إلى توسع القصبات وفشل الرئة.
س8: هل يصيب التليف الكيسي أعضاء غير الرئة؟
ج: نعم بشكل ملحوظ. يؤثر على البنكرياس (قصور في إنزيمات الهضم)، والكبد والمرارة، والجهاز الهضمي (انتفاخ وإسهال دهني)، والغدد العرقية، والجهاز التناسلي (عقم الذكور)، والمفاصل والعظام (هشاشة). لهذا تتطلب رعايته فريقاً طبياً متعدد التخصصات.
س9: ما هو مرض السكري المرتبط بالتليف الكيسي وكيف يختلف عن السكري العادي؟
ج: هو نوع فريد يجمع بين نقص الأنسولين (بسبب تليف البنكرياس وفقدان خلايا الجزيرة) ومقاومة الأنسولين في آنٍ واحد. يختلف عن النوعين الأول والثاني ولا يستجيب لخافضات السكر الفموية، بل يُعالج بأنسولين. يبدأ غالباً في العقد الثاني أو الثالث ويستلزم فحصاً سنوياً من عمر العاشرة.
س10: هل التليف الكيسي يسبب العقم؟
ج: عند الذكور نعم في تقريباً جميع الحالات، بسبب الغياب الخلقي الثنائي للأسهر (CBAVD). لكن إنتاج الحيوانات المنوية طبيعي عادةً، مما يتيح الإنجاب عبر استخراج الحيوانات المنوية والحقن المجهري. عند الإناث تقل الخصوبة لكن الحمل ممكن وأصبح شائعاً لدى من يتمتعن بوظائف رئة مستقرة.
س11: ما هي معدلات CFTR وكيف تعمل؟
ج: هي أدوية ثورية تستهدف الخلل الأساسي في بروتين CFTR بدلاً من علاج الأعراض فقط. نوعان رئيسيان: المُصحِّحات (تساعد البروتين المعطوب على الوصول لسطح الخلية)، والمُقوِّيات (تحسن فتح قناة الكلوريد). العلاج الثلاثي Trikafta يجمع كليهما ويشمل 90% من المرضى.
س12: ما هو دواء Trikafta وهل هو متاح للجميع؟
ج: Trikafta (Elexacaftor/Tezacaftor/Ivacaftor) هو العلاج الثلاثي الأكثر تأثيراً، معتمد لمن لديهم أليل F508del واحد على الأقل (≈90% من المرضى) من عمر 6 أشهر فما فوق. يحسن FEV1 بـ10-15 نقطة مئوية ويقلل التفاقمات بأكثر من 60%. تحدٍّ كبير: تكلفته العالية تُقيّد وصوله في دول كثيرة.
س13: ما هي تقنيات تصفية المسالك الهوائية ولماذا هي ضرورية يومياً؟
ج: هي تقنيات علاجية تساعد على إخراج المخاط المتراكم من الرئتين، تشمل: العلاج الطبيعي للصدر، أجهزة PEP المتذبذبة (Flutter وAcapella)، وسترات اهتزاز جدار الصدر. تُمارَس يومياً من 1-4 ساعات وتُعدّ العمود الفقري للرعاية التنفسية حتى مع توفر المعدلات.
س14: متى تصبح زراعة الرئة ضرورة في التليف الكيسي؟
ج: تُناقش حين ينخفض FEV1 إلى أقل من 30% من المتوقع، أو عند التدهور السريع رغم العلاج الأمثل، أو عند تكرر نفث الدم الخطير. نسبة البقاء بعد الزراعة تتجاوز 70% عند 5 سنوات، مع الحاجة لمتابعة متعددة التخصصات لعلاج مضاعفات التليف الكيسي غير الرئوية.
س15: هل التليف الكيسي يؤثر على الصحة النفسية؟
ج: نعم بشكل ملحوظ. يعاني 30-40% من المراهقين والبالغين المصابين من الاكتئاب أو القلق، نتيجة عبء العلاج اليومي المرهق والمرض المزمن. أصبح الفحص النفسي معياراً رسمياً في مراكز رعاية التليف الكيسي، وتُسهم الخدمات النفسية المتكاملة في تحسين الالتزام بالعلاج.
س16: ما الفرق بين التفاقم الرئوي والحالة المستقرة في التليف الكيسي؟
ج: الحالة المستقرة تعني أعراضاً محدودة ووظائف رئة ثابتة. التفاقم هو تدهور حاد يتميز بزيادة السعال وحجم البلغم وضيق التنفس والتعب وانخفاض FEV1، يستلزم علاجاً سريعاً بمضادات حيوية وريدية أو استنشاقية. التفاقمات المتكررة تُسرّع تدهور الرئة على المدى البعيد.
س17: ما الدور الغذائي في إدارة التليف الكيسي؟
ج: التغذية المثالية مرتبطة مباشرةً بجودة وظائف الرئة. يحتاج المرضى إلى 110-200% من السعرات الحرارية اليومية الموصى بها عالية الدهون، مع تناول إنزيمات البنكرياس (PERT) مع كل وجبة. نقص التغذية يُضعف المناعة ويُسرّع التدهور الرئوي، لذا يُعدّ التغذوي عضواً أساسياً في فريق الرعاية.
س18: هل CRISPR وتحرير الجينات قادران على علاج التليف الكيسي مستقبلاً؟
ج: هذا هو الأمل الأكبر. تقنية CRISPR-Cas9 ومحررات القواعد تخضع حالياً لتجارب سريرية تهدف لتصحيح طفرات CFTR على المستوى الجينومي مباشرةً. إذا نجحت ستوفر علاجاً لمن لا يستجيبون للمعدلات الحالية، وقد تكون أقرب للشفاء الحقيقي. التوقعات واعدة لكن التطبيق السريري الواسع لا يزال يحتاج وقتاً.
س19: هل يمكن للمصاب بالتليف الكيسي العيش حياة طبيعية؟
ج: بدرجة كبيرة نعم، خاصة في عصر معدلات CFTR. يتجاوز متوسط العمر المتوقع اليوم 50 عاماً في بيئات الرعاية المتقدمة، ويلتحق كثيرون بالجامعات ويعملون ويتزوجون ويُنجبون. التحدي الرئيسي هو الروتين العلاجي اليومي (2-4 ساعات) وإدارة التفاقمات وضرورة المتابعة الدورية المستمرة.
س20: ما الفحوصات الدورية الضرورية لمريض التليف الكيسي؟
ج: تشمل: قياس وظائف الرئة (FEV1)، زراعة البلغم لرصد البكتيريا، فحوصات الدم لوظائف الكبد والفيتامينات، كثافة العظام، اختبار تحمل الجلوكوز سنوياً (من عمر 10 سنوات) للكشف عن سكري التليف الكيسي، والتصوير بالأشعة المقطعية لتقييم توسع القصبات. كل هذه الفحوصات ركيزة أساسية للرعاية الوقائية.

تتميز مجموعة تركيا للرعاية الصحية بوجود فريق من خبراء الطب المتميزين، يسعون دائمًا لتقديم أفضل الخدمات الصحية للمرضى بأعلى معايير الجودة والاحترافية.
إذا كنت تبحث عن رعاية صحية متميزة أو تحتاج إلى استشارة طبية، فلا تتردد في التواصل معنا . ندعوك لمشاهدة كادرنا الطبي والتعرف على مؤهلاتهم وخبراتهم عن قرب.